బిస్మత్
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bismuth | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronunciation | /ˈbɪzməθ/ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Appearance | lustrous silver | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standard atomic weight Ar°(Bi) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bismuth in the periodic table | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Group | మూస:Infobox element/symbol-to-group/format | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Period | period 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Block | p-block | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electron configuration | [Xe] 4f14 5d10 6s2 6p3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrons per shell | 2, 8, 18, 32, 18, 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical properties | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase at STP | solid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point | 544.7 K (271.5 °C, 520.7 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Boiling point | 1837 K (1564 °C, 2847 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Density (near r.t.) | 9.78 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| when liquid (at m.p.) | 10.05 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of fusion | 11.30 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of vaporization | 179 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar heat capacity | 25.52 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Vapor pressure
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic properties | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidation states | −3, −2, −1, 0,[3] +1, +2, +3, +4, +5 (a mildly acidic oxide) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativity | Pauling scale: 2.02 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionization energies |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic radius | empirical: 156 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Covalent radius | 148±4 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals radius | 207 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Other properties | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Natural occurrence | primordial | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
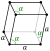
| Crystal structure | rhombohedral[4] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Speed of sound thin rod | 1790 m/s (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal expansion | 13.4 µm/(m⋅K) (at 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal conductivity | 7.97 W/(m⋅K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrical resistivity | 1.29 µΩ⋅m (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetic ordering | diamagnetic | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young's modulus | 32 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 12 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bulk modulus | 31 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson ratio | 0.33 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs hardness | 2.25 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell hardness | 94.2 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Number | 7440-69-9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| History | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Discovery | Claude François Geoffroy (1753) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes of bismuth | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Template:infobox bismuth isotopes does not exist | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
మౌలిక సమాచారం
మార్చుబిస్మత్ ఒక రసాయనిక మూలకం. బిస్మత్ మూలకాల ఆవర్తన పట్టికలో 15 సమూహము, p- బ్లాకు, 6వ అవధి/పీరియడ్నకు చెందిన లోహం.మూలకం యొక్క సంకేత అక్షరంBi. బిస్మత్ ఒక పెంటవాలెంట్ పోస్ట్ ట్రాన్సిసన్ లోహం. బిస్మత్ రసాయనికంగా ఆర్సెనిక్, ఆంటిమొని మూలకాలను పోలివున్నది. బిస్మత్ మూలకరూపంలో ప్రకృతిలో లభించినప్పటికీ, ఎక్కువగా సల్పైడ్, ఆక్సైడ్ ముడిఖనిజ రూపంలో లభిస్తుంది.
చరిత్ర
మార్చుబిస్మత్ అనాదిగా మానవునికి పరిచయముండుట వలన దీనిని మొదట ఎవరు లోహంగా గుర్తించినది చెప్పటం కష్టం. సా.శ.1546 లో "De Natura Fossilium" అనే గ్రంథంలో ఈ లోహం సీసం, తగరం కన్న భిన్నమైన లోహంగా అగ్రికోలా పేర్కొన్నాడు. 1738 లో జోహన్ హేన్రిచ్ పాట్ (Johann Heinrich Pott ), కార్ల్ విల్హెం స్కిలే (Carl Wilhelm Scheele, టి.ఒ.బెర్గమాన్ (Torbern Olof Bergman) తదితరులుసీసము (మూలకము), తగరం కన్న బిస్మత్తు భిన్నమైన లోహమని గుర్తించారు.1753 లో క్లాడ్ ఫ్రాన్కిస్ జియోఫ్రాయ్ (Claude Françంis Geoffroy ) బిస్మత్ లోహం, సీసం, తగరం లకన్నా భిన్నమైనదని ప్రత్యక్షంగా ప్రదర్శించి చూపాడు.[5] కత్తులను తయారు చేయుటలో కంచుమిశ్రమ దాతువుతో కలిపి ఉపయోగిస్తారు.
వనరులు –ఉత్పత్తి
మార్చుభూమిలో బిస్మత్ బంగారానికి రెండింతలు పరిమాణంలో లభిస్తుంది. బిస్మత్ యొక్క ముఖ్యమైన ఖనిజాలు బిస్మథైనైట్ (bismuthinite ), బిస్మైట్ (bismite) లు. దేశియ వనరులు ఆస్ట్రేలియా , బొలీవియా, చైనా దేశాలు. సంయుక్త రాష్ట్రాల జియోలోజికల్ సర్వే ప్రకారం 2010 లో ప్రంపంచ వ్యాప్తంగా 8,900 టన్నులు ఉత్పత్తి జరిగినది . అందులో సింహభాగం చైనా (6,500 టన్నులు, పెరు (1,100 టన్నులు ), మెక్సికో (850 టన్నులు ) దేశాలది. సీసం, రాగి, తగరం, మోల్బిడెనం, టంగ్స్టన్ లోహాల ఉత్పత్తిలో బిస్మత్ ఉప ఉత్పత్తి (by product ) గా లభిస్తుంది.
భౌతిక గుణాలు
మార్చుబిస్మత్ పెలుసైన లోహం. రంగు వెండిలా తెల్లగా ఉండును. ఉత్పత్తి అయిన వెంటనే వెండిలా తెల్లని రంగు కలిగి ఉన్నప్పటికీ, లోహం ఉపరితలం ఆక్సిజన్ తో ఆక్సీకరణ ఫలితంగా కొద్దిగా పింకు రంగుగా కనిపించును. బిస్మత్ ఒక డైయమగ్నేటిక్ మూలకం.అనగా దీనిపై ప్రయోగించిన అయస్కాంత క్షేత్రానికి 180° కోణంలో అయస్కాంత గుణము ప్రదర్శించును. ఇది పాదరసం మినహాయించి మిగతా అన్ని లోహాలకన్న తక్కువ ఉష్ణవాహక విలువ కలిగిన లోహం.[6] మూలకం యొక్క పరమాణు సంఖ్య 83. పరమాణు భారం :208.98040.
బిస్మత్ మూలకానికి కూడా నీటికున్న ఒక ప్రత్యేక లక్షణం కలిగి ఉంది. నీరు ఉష్ణోగ్రత తగ్గుతున్నప్పుడు 4 °C వరకు సంకోచిస్తుంది, అంతకన్న తగ్గేకొలది వ్యాకోచించును. బిస్మత్ కూడా తన గ్రూప్/సమూహంలోని సిలికాన్, gallium, ఆంటిమొని, జెర్మెనియం లకు భిన్నంగా, ఇది మాత్రం ఘనీభవించు ఉష్ణోగ్రత వద్ద వ్యాకోచించును[7] బిస్మత్ను ఆక్సిజన్తో మండించిన బిస్మత్ నీలిమంటతో మండగా, దీని ఆక్సైడ్ పూత పసుపురంగు పొగలను వెలువరించును. దీని విష ప్రభావాన్నిఆవర్తన పట్టికలో పొరుగు ములకాలైన సీసం, అంటిమోని, పొలోనియం లతో పోల్చిన, వాటికన్న బాగా తక్కువ. బిస్మత్ యొక్క విద్యత్ప్రవాహ నిరోధతత్త్వం చాలా అధికం. దీనిని పలుచని పొరలుగా ఆధారం మీద వుంచిన సెమి కండక్టరుగా పనిచేయును.
బిస్మత్ మూలకం భౌతిక ధర్మాల పట్టిక [7]
| భౌతిక ధర్మం | విలువ |
| రంగు | వెండిలా తెలుపు |
| భౌతికస్థితి | ఘనస్థితి |
| పరమాణుభారం | 208.9804 |
| ద్రవీభవన స్థానం | 271.4 °C, 544.5 K |
| మరుగు స్థానం | 1564 °C, 1837 K |
| ఎలక్ట్రాన్లసంఖ్య | 83 |
| ప్రోటాన్ల సంఖ్య | 83 |
| సాంద్రత @ 20 °C | 9.807 గ్రాం/సెం.మీ3 |
రసాయనిక చర్యలు
మార్చుసాధారణగది ఉష్ణోగ్రత వద్ద పొడి లేదా తడిగాలితో బిస్మత్ ఎటువంటి రసాయనిక చర్యకు లోను కాదు. ఎరుపెక్కునట్లు వేడిచేసిన నీటితో రసాయనచర్యలో పాల్గొని బిస్మత్ (iii ) ఆక్సైడ్ను ఏర్పరచును.
2Bi + 3H2O → Bi2O3 + 3H2
బిస్మత్ ప్లోరైడ్తో తక్కువ, ఎక్కువ (500 °C) ఉష్ణోగ్రత వద్ద చర్య జరుపును.500 °C వద్ద చర్య వలన బిస్మత్ (V ) ప్లోరైడ్, తక్కువ ఉష్ణోగ్రతవద్ద చర్యవలన బిస్మత్ (iii) ప్లోరైడ్ ఏర్పడును.100°Cపైన బిస్మథ్ ఫ్లోరైడ్ (BiF3) కు అదనంగా ఒక ఫ్ళోరైడ్ అణువు చేర్చబడిBiF5) ఏర్పడును. హలోజనులతో చర్య జరుపుట వలన బిస్మత్ (iii) హెలాయిడులు ఏర్పడును. ట్రై హెలాయిడులు లోహాలను క్షయింపచేయు లక్షణం (corrosive) కలవి, తేమతో త్వరితంగా చర్యలో పాల్గొని ఆక్సి హెలాయిడులను ఏర్పరచును[8].వీటి సంకేతం: BiOX
2Bi + 3X2 → 2BiX3 (X = F, Cl, Br, I)
బిస్మత్ గాఢ సల్పురిక్ ఆమ్లంలో కరిగి బిస్మత్ (iii) సల్పేట్, సల్పర్ డైఆక్సైడ్లను ఏర్పరచును.
6H2SO4 + 2Bi → 6H2O + Bi2 (SO4) 3 + 3SO2
నత్రికామ్లంతో రసాయనిక చర్య వలన బిస్మత్ (iii) నైట్రేట్ ఏర్పరచును.
Bi + 6HNO3 → 3H2O + 3NO2 + Bi (NO3) 3
ఆక్సిజన్ సమక్షములో హైడ్రోక్లోరిక్ ఆమ్లంలో కరిగి చర్య జరుపుట వలన బిస్మత్ క్లోరైట్ ఏర్పరచును[8].
4Bi + 3O2 + 12HCl → 4BiCl3 + 6H2O
క్షారమృత్తిక లోహ సంయోగపదార్థసమూహాలను (complexes) ఏర్పరచుటకు బిస్మత్ నులోహ పరివర్తన కారకం ( transmetalating) గా ఉపయోగించడం జరుగుతుంది.
3Ba + 2BiPh3 → 3BaPh2 + 2Bi
బిస్మత్ రసాయనిక సమ్మేళనాలు
మార్చుబిస్మత్ ట్రై వాలెంట్, పెంటా వాలెంట్ సమ్మేళనాలను ఏర్పరచును.ముఖ్యంగా ట్రై వాలెంట్ సమ్మేళన పదార్థాలను ఏర్పరచడం ఎక్కువ. బిస్మత్ యొక్క చాలా రసాయనిక లక్షణాలు ఆర్సెనిక్, అంటిమోని లను పోలి ఉండును.
ఆక్సైడులు ,సల్పైడులు
మార్చు- ఎక్కువ ఉష్ణోగ్రత వద్ద బిస్మత్ లోహపు ఆవిరులు వేగంగా చురుకుగా అక్సిజనుతో సమ్మేళనం చెందటం వలన పసుపువర్ణపు బిస్మత్ ట్రైఆక్సైడ్ ఏర్పడును (Bi2O3). ఈ ఆక్సైడ్ 710 °C వద్ద ద్రవస్థితిలో ఉండగా ఎటువంటి లోహఆక్సైడ్నైన హరించి వేయును (Corrosive, ప్లాటినంఆక్సైడ్ను కూడా క్షయింపజేయును.
- క్షారాలతో చర్య వలన ఆక్సి ఆనయానులను విడుదల చేయును. BiO2 అనేది బహుజాతీయము (polymeric}, ఇది నిడువైన గొలుసాకృతి BiO3−3ను సృష్టించును. Li3BiO3 అనేది ఘనాకృతి ఆక్టామెరిక్ /అష్టరూప ఆనయాను. Na3BiO3 etrameric. ముదురు/చిక్కని ఎరుపు బిస్మత్ (v) ఆక్సైడ్ (BiO5, అస్థిరమైనది, వేడి చేసినచో ఆక్సిజన్ను విడుదల చేయును .
- NaBiO3 సమ్మేళనం ఒకఆమ్లజనీకరణ పదార్థము (oxidising agent). బిస్మత్ సల్పైడ్ Bi2S3స్వాభావికంగా బిస్మత్ ముడిఖనిజంతో పాటు లభిస్తుంది.ద్రవబిస్మత్, సల్ఫరుల మిళనం వలన బిస్మత్ సల్పైడ్ను ఉత్పత్తి చేయవచ్చును.
బిస్మథైన్ , బిస్మథైడ్
మార్చుబిస్మత్ యొక్క హైడ్రైడ్లు స్థిరమైనవి కావు. బిస్మత్ హైడ్రైడ్, బిస్మథైన్ (bismuthine (BiH3) ఏర్పడునప్పుడు జరుగు రసాయనికచర్య ఉష్ణగ్రాహక (endothermic) ప్రతి చర్య.అనగా చర్యాకాలంలో ఉష్ణం గ్రహింపబడుతుంది, ఇలా ఏర్పడిన సమ్మేళనం గది ఉష్ణోగ్రత వద్ద ఉభయవియోగం చెందుతుంది. ఇది - (minus )60౦C వద్ద మాత్రమే స్థిరంగా ఉండును. బిస్మథైడ్ (bismuthide) లు బిస్మత్, ఇతర లోహాల అంతర్లోహ (intermetallic) సమ్మేళనాలు.
ఐసోటోపులు(isotopes)
మార్చుమొదట Bi -209 ని భారమైన స్థిరమైన ఐసోటోపుగా తలంచారు.కాని 2003 లో పూర్తిగా స్థిరమైనది కాదని ఇది అల్పా కిరణాలను వెలువరించడం వలన గుర్తించారు.Bi-209 ఆల్పా కిరణాల క్షయికరణ అర్ధజీవితకాలము 1.9X1019సంవత్సారాలని తేలినది.ఈ సమయం విశ్వంవయస్సు కన్న బిలియనురెట్లు ఎక్కువ.[9]
బిస్మత్-209 అతి ఎక్కువ అర్ధజీవితకాలం కలిగిన స్థిరమైన భారలోహం, రేడియో ధార్మికతరహితం అగుట మూలాన, దీనిని వైద్య, పారిశ్రామిక రంగంలో బిస్మత్-209 ను విస్తృతంగా వాడెదరు.
బిస్మత్ మూలకం యొక్క ఐసోటోపుల అర్ధజీవిత కాలపట్టిక[10]
| ఐసోటోపులు | అర్ధజీవితకాలం | ఐసోటోపులు | అర్ధజీవితకాలం |
| Bi-202 | 1.7గంటలు | Bi-210 | 5.0రోజులు |
| Bi-204 | 11.2గంటలు | Bi-21m | 3000000 ఏండ్లు |
| Bi-205 | 15.3రోజులు | Bi-211 | 2.1నిమిషాలు |
| Bi-206 | 6.24రోజులు | Bi-212 | 1.0గంట |
| Bi-207 | 32.0ఏండ్లు | Bi-213 | 45.6నిమిషాలు |
| Bi-208 | 368000ఏండ్లు | Bi-214 | 19.9 నిమిషాలు |
| Bi-209 | స్థిరం | Bi-215 | 7.0నిమిషాలు |
రేడియాన్ని లీనియరు పార్టికిల్ అక్సిలేటరు నుండి వెలువడిన bremsstrahlung ప్రోటానులతో బలంగా ఢీకొట్టింఛడం/తాటించడం వలన bismuth-213ను సృష్టించవచ్చును.దీని అర్ధజీవితకాలం 45 నిమిషాలు.అల్ఫాకణాలు మెటీరియల నుండి వెలువడగానే నశించును. దీనిని ల్యూకేమియ (leukemia) చికిత్సలోవాడెదరు.అంతేకాదు కాన్సరు చికిత్సలోTAT (targeted alpha therapy ) పొగ్రామ్లో వాడిచూసారు[11][12]
ఉపయోగాలు
మార్చుబిస్మత్ సమ్మేళనాలను ఎక్కువగా సౌందర్య సాధనాలలో, రంగులలో, స్వల్ప ప్రమాణంలో ఔషదాల తయారీ పరిశ్రమలలో వినియోగించుచున్నారు. ముఖ్యంగా పెప్టో –బిస్మోల్ను అతిసారం నిరోదినిగా వాడెదరు. బిస్మత్ తక్కువ విషకారక గుణం కల్గి ఉన్నందున, ముద్రణ అచ్చులను చేయుటకు (casting of printing type ) సీసం బదులుగా బిస్మత్తును ఉపయోగించం పెరిగింది. బిస్మత్తు ఉత్పత్తిలో మూడులో ఒకటవ వంతును ఈ అచ్చుల తయారీలో ఉపయోగిస్తున్నారు .
ఇవికూడా చూడండి
మార్చుమూలాలు
మార్చు- ↑ "Standard Atomic Weights: Bismuth". CIAAW. 2005.
- ↑ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; et al. (2022-05-04). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry (in ఇంగ్లీష్). doi:10.1515/pac-2019-0603. ISSN 1365-3075.
- ↑ Bi(0) state exists in a N-heterocyclic carbene complex of dibismuthene; see Deka, Rajesh; Orthaber, Andreas (May 6, 2022). "Carbene chemistry of arsenic, antimony, and bismuth: origin, evolution and future prospects". Royal Society of Chemistry. 51 (22): 8540–8556. doi:10.1039/d2dt00755j. PMID 35578901. S2CID 248675805.
- ↑ Cucka, P.; Barrett, C. S. (1962). "The crystal structure of Bi and of solid solutions of Pb, Sn, Sb and Te in Bi". Acta Crystallographica. 15 (9): 865. doi:10.1107/S0365110X62002297.
- ↑ "The Element Bismuth". education.jlab.org. Retrieved 2015-03-26.
- ↑ "Chemical properties of bismuth". lenntech.com. Retrieved 2015-03-26.
- ↑ 7.0 7.1 "Bismuth Element Facts". chemicool.com. Retrieved 2015-03-26.
- ↑ 8.0 8.1 "Organobismuth Chemistry". books.google.co.in. Retrieved 2015-03-27.
- ↑ "SAO/NASA ADS Physics Abstract Service". adsabs.harvard.edu. Retrieved 2015-03-27.
- ↑ "Periodic Table Bismuth". chemicalelements.com. Retrieved 2015-03-26.
- ↑ Imam, S (2001). "Advancements in cancer therapy with alpha-emitters: a review". International Journal of Radiation Oncology Biology Physics. 51: 271. doi:10.1016/S0360-3016(01)01585-1.
- ↑ Acton, Ashton (2011). Issues in Cancer Epidemiology and Research. p. 520. ISBN 978-1-4649-6352-0.